Der systematische Name eines Alkans kann mittels einfacher Regeln ermittelt werden. Diese Regeln stellen die Grundlage für die Benennung komplexerer Moleküle dar, weshalb man sich etwas Zeit nehmen sollte um die Nomenklatur der Alkane zu verstehen. Ich werde am Anfang die Grundlagen einmal ausführlich mit Beispielen erklären. Falls du nur nochmal einen Überblick brauchst, schau dir direkt die Zusammenfassung an und probiere dich an den Übungsbeispielen.
Grundlagen der Benennung
Was sind Alkane?
Alkane sind sogenannte gesättigte Kohlenwasserstoffe. Es handelt sich also um Verbindungen die nur aus Kohlenstoff- und Wasserstoffatomen bestehen und keine Doppelbindungen aufweisen.
Auswahl der längsten Kette
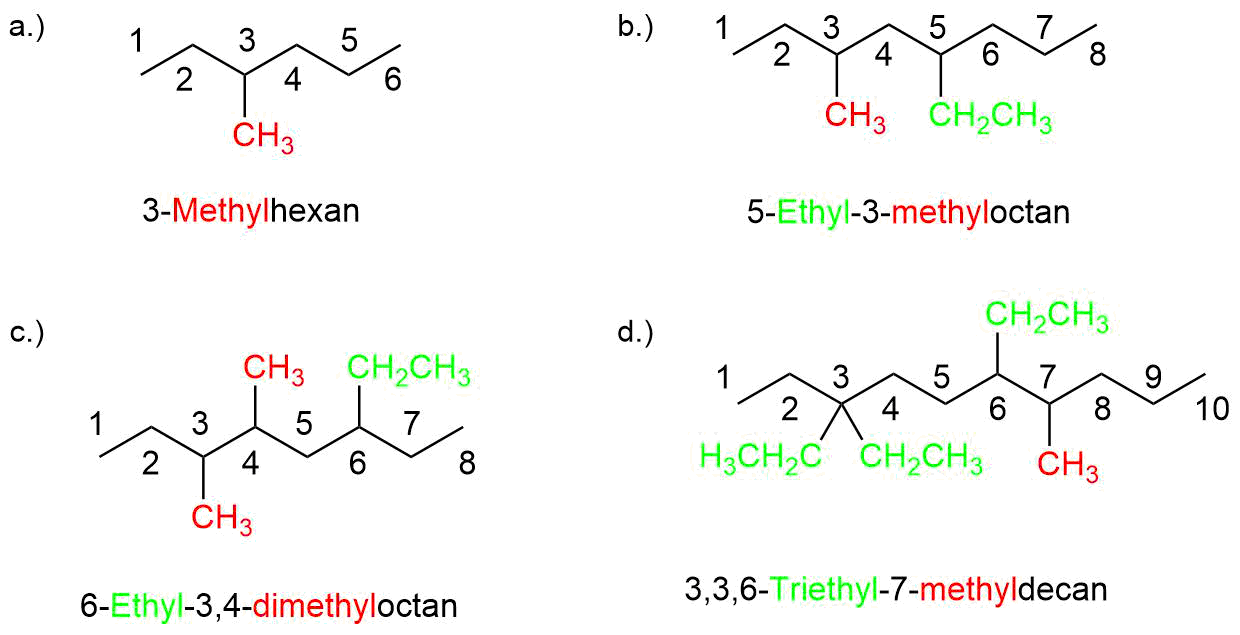
Am Anfang muss die längste ununterbrochene Kohlenstoffkette des Moleküls gefunden werden. Dies kann sich teilweise als schwierig erweisen, da die längste Kette nicht zwangsweise eine gerade Kette sein muss. Es kann vorkommen, dass man auch mal “abbiegen” muss, um die längste durchgehende Kette zu erhalten. Schauen wir uns dies mal an Beispielen an, wobei jeweils die längste Kette in rot markiert wurde.

Hat man die längste Kette gefunden, bestimmt man ihren Namen. Dies tut man, indem man die Kohlenstoffatome zählt und dann schaut, welchem Alkan aus der homologen Reihe sie entsprechen. Bei unseren Molekülen sind es jeweils acht Kohlenstoffatome und somit stellt Octan unsere Hauptkette da.
Benennung von verzweigten Alkanen
Woher kommt die Endung yl-?
Die Abzweigungen erhalten anstelle der Endung “an” (Methan) die Endung “yl” (Methyl). Man entfernt hierbei gedanklich ein Wasserstoffatom vom entsprechenden Alkan und erhält so eine Alkyl-Gruppe.
Nun betrachten wir einen Substituenten (z.B eine Methyl- oder eine Ethylgruppe) der von unserer Hauptkette abzweigt. Der Name dieses Substituenten wird vor den Namen unserer Hauptkette mit der entsprechenden Zahl geschrieben. Die Zahl beschreibt hierbei die Lage des Substituenten.
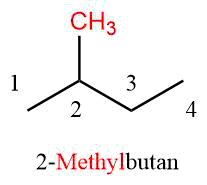
Die Nummerierung erfolgt jedoch nicht willkürlich sondern so, dass der Substituent die kleinste mögliche Zahl erhält.

Wenn verschiedene Substituenten vorliegen erfolgt die Auflistung so, dass die Substituenten insgesamt die kleinstmögliche Bezifferung erhalten.

Wenn du dir mal nicht sicher bist, addiere einfach mal die Ziffern zusammen. Probieren wir es am 2,2,4-Trimethylhexan (oben) aus. Für die falsche Benennung ergibt sich die Zahl 13 (3+5+5) und für die richtige Benennung die Zahl 8 (2+2+4). Du kannst die richtige Bezifferung also an der kleineren Zahl erkennen. Du kannst es ja mal an dem anderen Molekül ausprobieren.
Besondere Alkylreste...
Für einige Alkylsubstituenten haben sich spezielle Bezeichnungen etabliert, welche sich als praktisch erwiesen haben, aber leider für den Moment auswendig gelernt werden müssen. Diese Namen folgen jedoch einer gewissen Systematik, welche wir uns später nochmal genauer ansehen werden.

Diese “Bausteinen” können nun genutzt werden um Alkane mit verzweigten Resten zubenennen.

Die alphabetische Aufzählung
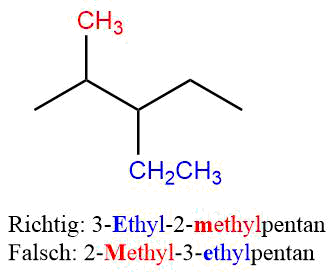
Die Substituenten werden alphabetisch und unabhängig von den Ziffern angegeben. Falls ein Substituent mehrfach vorliegt werden die Vorsilben “Di-” ,”Tri-” ,”Tetra-” und so weiter genutzt um anzugeben, wie oft der Substituent vorliegt.
Die Anzahl der angegeben Ziffern muss der Vorsilbe entsprechen, d.h. dass bei der Vorsilbe “Di” zwei Ziffern, bei “Tri” drei usw. angegeben werden müssen. Hier ein kleines Beispiel…

Diese Vorsilben beeinflussen jedoch nicht die alphabetische Reihenfolge! Hierbei werden nur die Vorsilben “Cyclo-” und “Iso-” beachtet.
Sonderfall: Beide Abzählrichtungen ergeben die selbe Bezifferung
Es kommt auch mal vor, dass sich in beiden Abzählrichtungen die gleiche Summe ergibt…
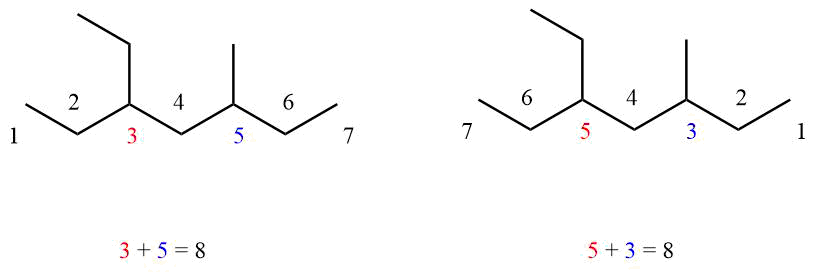

In diesem Fall bekommt der Substituent der zuerst im Alphabet kommt die niedrigere Ziffer. In unserem Beispiel wäre das also die Ethylgruppe.
Alkane vs Cycloalkane
Sobald sich Ringe innerhalb der Verbindung befinden muss man aufpassen. In diesem Fall stellt sich nehmig die Frage nach der Grundstruktur. Falls der Ring eine höhere Anzahl an Kohlenstoffatomen aufweist als die längste Kette, muss die Nomenklatur der Cycloalkane verwendet werden. Andernfalls wird der Ring wie ein Substituent behandelt.
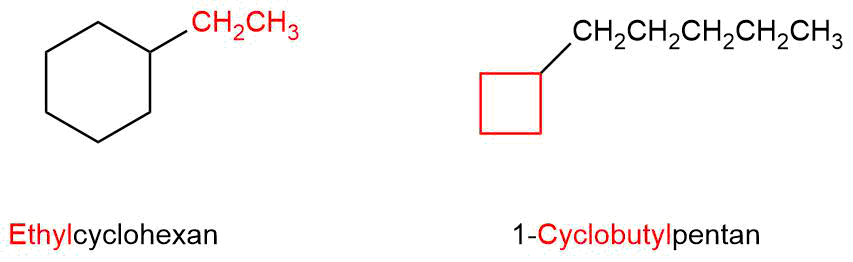
Nomenklatur der Halogenalkane
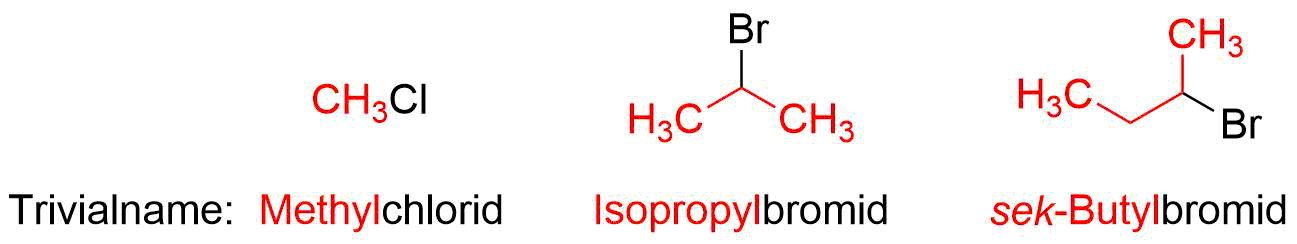
In der organischen Chemie kommen oftmals Halogenalkane zum Einsatz. In diesen werden formal Wasserstoffatome gegen Halogenatome (z.B Chlor oder Iod) ausgetauscht. Bei der Benennung werden die Halogenalkane wie substituierte Alkane behandelt. Wir können also die gleichen Regeln verwenden wie bei verzweigten Alkanen.

Häufig werden jedoch nur die Trivialnamen für einfache Halogenalkane verwendet. Diese setzen sich aus dem entsprechenden Alkylrest, gefolgt von dem Namen des Halogens mit der Endung “-id” zusammen.
Zusammenfassung der Nomenklatur der Alkane
Im folgenden gehen wir einmal die wichtigsten Schritte an einem Beispiel durch.
Step 1: Finde die längste Kette.

Step 2: Nummeriere die Kohlenstoffkette so, dass den Substituenten insgesamt die niedrigstmögliche Ziffer zufällt.

Step 3: Die Substituenten werden in alphabetischer Reihenfolge und mit den entsprechenden Ziffern und Vorsilben (“Di-” , “Tri-” , “Tetra-” usw.) vor den Namen der längsten Kette geschrieben.

Übungen mit Lösungen
Hier findest du einige Übungen mit Lösungen zur Nomenklatur der Alkane.
Benennung von Strukturen...
Wie werden die folgenden Strukturen benannt?
Zeichne die zugehörigen Strukturen…
Literatur
Weitere Informationen zu diesem Thema kannst du in den folgenden Büchern finden.
J. Clayden, N. Greeves, S. Warren: Organische Chemie. Springer Spektrum; 2. Auflage, 2013. *
- Paula Y. Bruice: Organische Chemie: Studieren kompakt. Pearson Studium, 5. Auflage, 2011. *
* bezahlter Link